La separazione della CO2 dai gas combusti
Dopo aver parlato delle tecniche di cattura e stoccaggio dell’anidride carbonica (CCS), entriamo nel dettaglio sul processo di separazione, ovvero come la CO2 viene separata da una miscela gassosa (quale quella formata dai gas combusti).
I processi di separazione della CO2 da miscele gassose
Le principali tecnologie utilizzate per la separazione della CO2 dalle miscele gassose sono divisibili in quattro tipologie:
- Processi di absorbimento
- Separazione mediante membrane
- Processi criogenici
- Processi di adsorbimento
Absorbimento
Il processo di absorbimento sfrutta solventi liquidi per separare la CO2 dalla miscela gassosa. È impiegato nell’industria petrolifera e del gas naturale e può essere di tipo chimico o fisico.
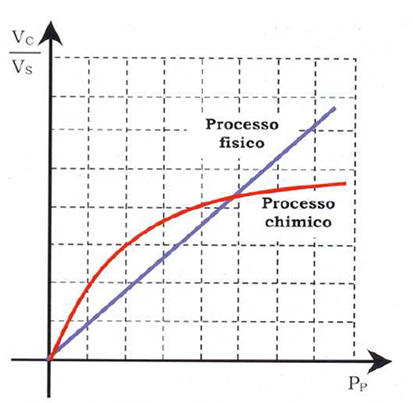
La differenza sostanziale tra absorbimento chimico e fisico consiste nella differente interazione tra il solvente e l’absorbato (in questo caso la CO2) e nella diversa relazione tra la pressione parziale del composto ed il rapporto tra il volume dell’absorbato ed il volume del solvente.
Come si può osservare dal grafico infatti, a basse pressioni conviene sfruttare un processo chimico, che garantisce una maggiore cattura di CO2 mentre ad alte pressioni conviene l’utilizzo di un processo fisico.

Absorbimento chimico
Nell’absorbimento chimico la CO2 forma un composto intermedio con il solvente mediante legami chimici deboli che vengono poi spezzati dal processo rigenerativo del solvente.
Tra i solventi più sfruttati si annoverano: le ammine come la DiEtanolAmmina (DEA) o la MonoEtanolAmmina (MEA), l’ammoniaca, il carbonato di sodio, il carbonato di potassio o l’idrossido di sodio.
Il processo di absorbimento mediante ammine può essere diviso in due stadi: l’absorbimento di CO2 e la rigenerazione del solvente. Nel primo una soluzione acquosa di ammina viene insufflata in controcorrente al flusso dei gas combusti contenenti l’anidride carbonica in una torre di assorbimento; in questo modo si massimizza la superficie di contatto e si migliora il mescolamento. Nel secondo la miscela entra in una colonna rigenerativa ad alte temperature; si rompono così i legami deboli tra ammina e CO2 e si cattura quest’ultima che viene inviata ad un impianto di liquefazione.
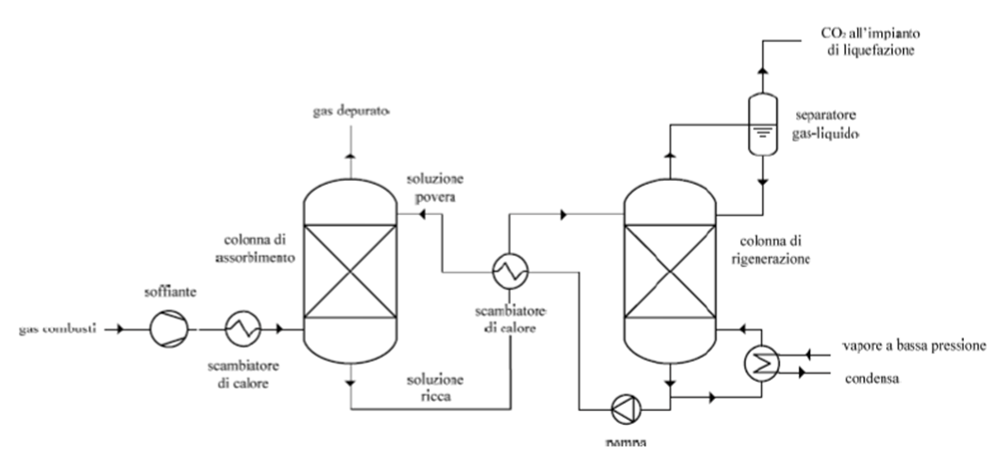

Schema di impianto absorbimento chimico
Le criticità principali di questo processo sono il grande quantitativo di solvente necessario (le ammine si degradano quindi ad ogni ciclo deve esserci un reintegro del solvente), la modesta quantità di CO2 rispetto all’unità di solvente e soprattutto l’elevata richiesta di energia termica per la rigenerazione del solvente.
Quest’ultimo aspetto è fondamentale perché influisce notevolmente sul bilancio del processo; i consumi di vapore per unità di massa di CO2 per la rigenerazione della soluzione sono di circa 3–4 MJ/kg.
Absorbimento fisico
Nel caso dell’absorbimento fisico la CO2 viene assorbita da un solvente che verrà rigenerato mediante riscaldamento e/o riduzione di pressione.
Il processo è regolato dalla legge di Henry secondo la quale la solubilità di un gas in un solvente fisico aumenta all’aumentare della pressione ed al diminuire della temperatura.
C = K * p
Dove viene indicata con C la concentrazione del gas nella soluzione, con p la pressione del gas sulla soluzione e k la costante tipica del gas che nel caso dell’anidride carbonica è:
k = 3.4×10^(-2) mol/(atm L)
Uno dei processi fisici più sfruttati è il Selexol che sfrutta come solvente il polietilene glicol dimetiletere ed il Rectisol che utilizza metanolo.
Come per il processo di absorbimento chimico anche il fisico può essere diviso in due stadi.
Nel primo stadio avviene l’absorbimento di CO2 a pressioni elevate (50–60 bar per il caso del Selexol), con lo scambio in controcorrente tra il flusso del gas di scarico contenente la CO2 e quello contenente il solvente.
Nel secondo stadio avviene la rigenerazione del solvente attraverso una riduzione di pressione in un processo denominato “Flash” dal nome delle camere di espansione dette appunto camere di flash.
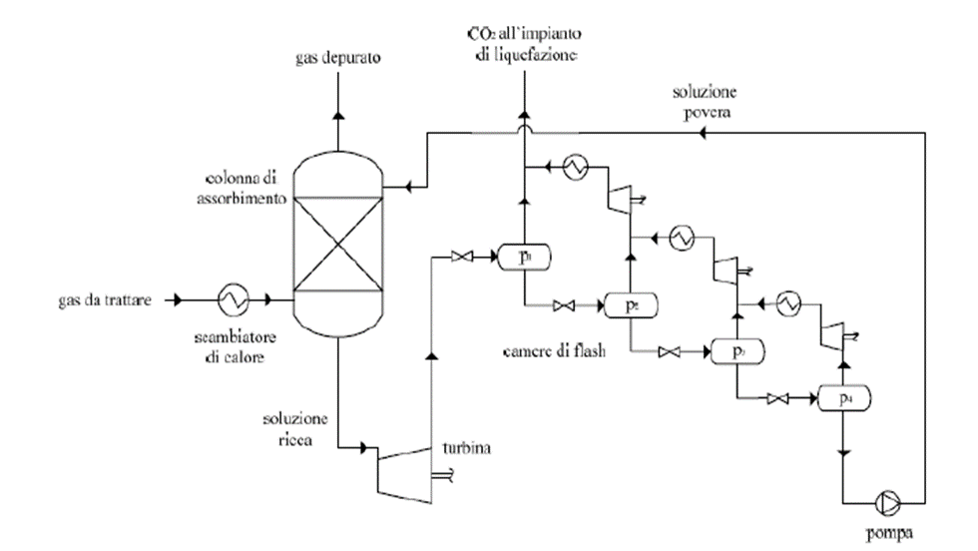

Schema di impianto absorbimento fisico
I vantaggi rispetto al processo chimico sono soprattutto in termini di costi, volumi ridotti ed all’assenza di fenomeni corrosivi. Inoltre al contrario delle ammine usate nel processo chimico il Selexol è scarsamente reattivo rispetto alle altre sostanze inquinanti “in uscita” dalla combustione quali SOx, NOx ed il particolato.
Di contro occorre considerare la necessità di mantenere la colonna di assorbimento ad alte pressioni, il che comporta una spesa energetica nel lavoro di compressione e nel raffreddamento a temperature inferiori a 0 °C per alcuni impianti ed una serie di problematiche progettuali legate alla sicurezza dell’impianto.
Separazione della CO2 mediante membrane
Il processo di separazione mediante membrane può essere classificato in base alla natura della separazione della CO2 dai gas combusti; possiamo individuare membrane a separazione di gas e membrane ad absorbimento.
Le prime sfruttano la differente diffusività e solubilità dei gas e la diverse interazioni tra i gas della miscela ed il materiale del quale è costituita la membrana. In questo caso si osserva che la CO2 attraversa più velocemente la membrana rispetto agli altri gas del flusso venendo così separata.
Le seconde consistono in membrane idrofobe microporose contenenti un liquido absorbente. L’anidride carbonica presente nella miscela gassosa diffonde attraverso i pori della membrana e viene assorbita dal lato opposto della membrana in maniera selettiva dal liquido absorbente. Il solvente viene poi rigenerato per separare l’absorbato catturato.
Processi criogenici
Questi processi prevedono la separazione criogenica della CO2 da una miscela gassosa ed avvengono mediante compressione e refrigerazione su differenti stadi. Comportano, di conseguenza, un cambiamento di fase della CO2 che viene portata in forma solida o liquida e successivamente separata mediante distillazione.
Il vantaggio più importante di questi processi sta nella grande capacità di recupero della CO2 ma i costi rendono il processo difficilmente sfruttabile in ambito industriale. La presenza di vapore acqueo inoltre porta alla formazione di ghiaccio che può creare problemi all’impianto pertanto è necessaria una deumidificazione della miscela gassosa, che deve essere anche priva di SOx, NOx e particolato.
Adsorbimento
L’adsorbimento è un fenomeno di attrazione molecolare superficiale che si verifica quando un adsorbente solido entra in contatto con un adsorbato liquido o gassoso.
Come per l’absorbimento, i materiali adsorbenti possono essere differenziati in base alla natura del processo che può essere fisico – fisisorbimento, o chimico – chemisorbimento. Mentre l’absorbimento riguarda l’intera massa in oggetto, adsorbimento è un fenomeno superficiale.
In particolare, una volta che i due composti entrano in contatto l’adsorbato viene adsorbito attraverso i pori del solido adsorbente per effetto di meccanismi di diffusione.
Altra caratteristica fondamentale di questo fenomeno è la spontaneità della reazione e la diminuzione dell’entropia della sostanza adsorbita. L’adsorbimento è quindi un processo esotermico e come tale, in seguito all’interazione tra i due “attori” del fenomeno, cede calore. Per quando riguarda invece il desorbimento, ovvero il processo rigenerativo del materiale adsorbente, è necessario fornire calore. Di conseguenza più debole è il legame tra adsorbato e adsorbente meno energia verrà spesa nella rigenerazione.
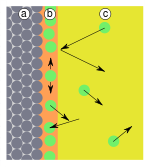

Adsorbimento fisico
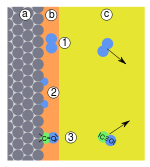

Adsorbimento chimico
Nelle figure si può notare la differenza tra il fenomeno chimico, nel quale avviene una reazione chimica sulla superficie del substrato, ed il fenomeno fisico.
I materiali adsorbenti solidi vengono selezionati principalmente in base alla loro affinità specifica con il soluto da adsorbire e dalle dimensioni dei pori.
Sono stati sfruttati come materiali adsorbenti solidi per la cattura di CO2: gli zeoliti, il carbone attivo, gel di silicio, nanotubi in carbonio, argille, l’allumina ed i suoi fosfati, resine, polimeri inorganici e materiali metallo – organici detti MOF (metal organic frameworks).
Negli ultimi anni numerose ricerche si sono concentrate sull’utilizzo di questi ultimi materiali, che grazie alle loro alte capacità adsorbenti potrebbero risultare una valida alternativa ai sistemi di absorbimento sfruttati fin ora.
Il processo del tipo fisisorbimento comporta interazioni deboli del tipo intermolecolare come i legami di van deer Waals. Per far sì che tale fenomeno sia “macroscopicamente rilevante” il materiale adsorbente dovrà esporre un’ampia superficie d’interfaccia, caratteristica di una forma pulverulenta del materiale.
In conclusione, il metodo più sfruttato per la cattura della CO2 è quindi l’absorbimento (sia esso chimico o fisico) ma il più promettente risulta essere l’adsorbimento in base alla scelta del materiale adsorbente. Nel prossimo articolo approfondiremo infatti l’utilizzo di materiali adsorbenti metallo-organici di tipo MOF per la cattura dell’anidride carbonica.
Fonti
- Immagine di copertina
- Cau G. – Cocco D. “L’Impatto Ambientale dei Sistemi Energetici”. SGEditoriali – IV Edizione – 2015
- CO2CRC