Batterie agli ioni di litio
Una pila, o più comunemente “batteria”, è un dispositivo che converte energia chimica in energia elettrica. Può essere usata sia come generatore di corrente sia come generatore di tensione a seconda dell’utilizzo.
Esistono moltissime tipologie di pile, possiamo distinguerle in due gruppi:
- batterie non ricaricabili o batterie primarie (quali per esempio le batterie AA)
- batterie ricaricabili o batterie secondarie o accumulatore di carica elettrica (quali per esempio quelle nei dispositivi elettronici)

Batteria AA

Batteria ricaricabile NiMH CS RS Pro NiMH
Il principio chimico-fisico alla base del funzionamento della pila è una reazione di ossidazione che avviene al suo interno. Il processo di ossidazione di una sostanza consiste nella perdita di elettroni della stessa, mentre un’altra sostanza che ha acquisito elettroni subisce un processo detto di riduzione. La struttura della pila consente di incanalare e, di conseguenza sfruttare, questo flusso di elettroni che si genera tra le due sostanze. La pila si scarica quando le reazioni che avvengono al suo interno raggiungono un equilibrio, ovvero quando la sostanza ad ossidarsi smette di cedere elettroni.
Breve storia della batteria
L ‘inventore della pila può essere considerato Alessandro Volta che nel 1799 riprendendo gli studi di Luigi Galvani sulla corrente elettrica, riuscì a realizzare la prima pila, oggi detta voltaica.
La pila di Volta consiste in dischetti di rame e zinco alternati, secondo lo schema rame-zinco-umido-rame-zinco, il tutto mantenuto verticalmente da una struttura di legno esterna. Una volta disposti i dischetti e il panno sul supporto, collegando il primo e l’ultimo dischetto della colonna con due fili di rame, si viene a creare tra essi una differenza di potenziale. La differenza di potenziale genera un flusso di elettroni che può essere fruttato attraverso i cavi di rame collegati alla pila.
Negli anni in molti hanno contribuito allo sviluppo di questa tecnologia tra i quali John Frederic Daniell, William Robert Grove e Robert Wilhelm Eberhard Bunsen (solo per citarne alcuni) fino ad arrivare alle pile di oggi.
Oggi sono molte le batterie di uso comune, le pile zinco-carbone, zinco-aria, alcaline, batterie di argento e tante altre. Le batterie che hanno segnato una svolta nell’elettronica, in particolare per quanto riguarda i dispositivi mobili, sono le batterie agli ioni di litio. Queste hanno permesso di ottenere una discreta quantità di energia immagazzinata in un ridotto spazio. Oggi infatti la maggior parte dei dispositivi elettronici portatili sfruttano queste tipologia di batteria per il proprio funzionamento, dispositivi quali tablet telefoni o computer portatili.
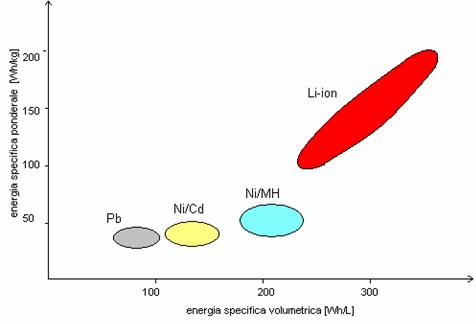
Differenza tra l’energia specifica legata alle dimensioni delle varie batterie e l’energia specifica prodotta dalla stessa
Batteria agli ioni di litio
I telefonini dei primi anni ’90 dello scorso secolo utilizzavano batterie realizzate con leghe al nichel-cadmio (Ni-Cad), l’evoluzione tecnologica ha portato allo sviluppo di batterie al litio più efficaci ed efficienti. Entrano dunque in scena le batterie agli ioni di litio, che assicurano prestazioni migliori, un tempo di ricarica inferiore e dimensioni più contenute rispetto alle pile della generazione precedenti. Esistono due tipologie di batterie al litio, quelle Li-Ion e quelle Li-po.
- Li-Ion (batterie agli ioni di litio), possono essere a forma di bottone o come lunghi cilindri metallici. I sali del minerale vengono immersi in un solvente liquido che funge da elettrolita (sostanze che subisce la suddivisione in ioni delle proprie molecole).
- Li-po (batterie ai polimeri di litio) il solvente liquido è sostituito da un composto polimerico (simile ad una plastica) solido, che rende gli accumulatori maggiormente modellabili e adattabili alle situazioni più disparate.
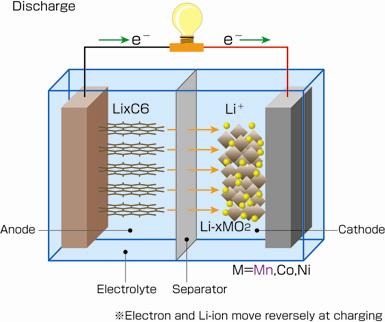
In entrambi i casi, il funzionamento delle batterie a litio si basa su delle reazioni chimiche: gli ioni di litio (Li+) si muovono dall’anodo in carbonio (elettrodo positivo) al catodo (elettrodo negativo). Il movimento prodotto dagli atomi rilascia energia all’intero circuito. Quando si mette in funzione il caricabatterie il processo è inverso, si fornisce energia che viene utilizzata per ridistribuire gli elettroni, quindi gli ioni positivi sono assorbiti dall’anodo.
I materiali più utilizzati per la costruzione dei catodi sono gli ossidi di Mn, Ni, Co, i quali presentano una struttura cristallina piuttosto aperta con canali e spazi all’ interno dei quali si inseriscono facilmente gli ioni di Litio, mentre per l’anodo è molto utilizzata la grafite. La grafite presenta una struttura a strati, con piani di atomi disposti in strutture esagonali fortemente legati tra loro , mentre i vari piani sono tenuti assieme da legami deboli.
La tensione generata agli estremi della batteria (catodo ed anodo) può essere calcolata attraverso la relazione empirica:
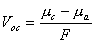
- µc è il potenziale di catodo
- µa è il potenziale di anodo
- F è la costante di Faraday
Vantaggi e svantaggi
Le batterie agli ioni di litio possono essere costruite in una vasta gamma di forme e dimensioni in modo da riempire efficientemente gli spazi disponibili nei dispositivi che le utilizzano.
Queste batterie sono più leggere delle equivalenti fabbricate con altri componenti chimici, perché gli ioni di litio hanno una densità di carica molto elevata, la più alta di tutti gli ioni che si sviluppano naturalmente. Gli ioni di litio sono piccoli, mobili e immagazzinabili facilmente. Inoltre una batteria basata sul litio è piccola e utilizzabile ovunque. Gli ioni necessitano di meno intermediari per l’immagazzinamento, cosicché è possibile destinare una quota maggiore di peso della batteria alla carica.
Le batterie Li-ion non soffrono dell’effetto memoria. Hanno anche un basso tasso di auto-scarica, circa il 5% mensile, ma soffrono di una lenta perdita permanente di capacità. Questo rappresenta uno dei principali svantaggi ovvero la batteria presenta un degrado progressivo anche se non viene utilizzata: ha una durata di conservazione fissa, in inglese shelf – life, a partire dal momento della fabbricazione, indipendentemente dal numero di cicli di carica/scarica.
Le batterie Li-ion non sono durature come quelle al nichel metal-idruro o al nichel-cadmio (precedenti batterie utilizzate nei telefoni degli anni ’90) e possono essere pericolose in caso di errato utilizzo in alcuni casi si gonfiano, in altri, più rari, esplodono creando non pochi problemi. Di solito sono anche più costose, infatti il problema delle batterie a base di litio è l’approvvigionamento della materia prima: il litio è disponibile in natura in quantità limitata e richiede processi di estrazione particolarmente complicati e costosi.

batteria agli ioni di litio espansa
Per i motivi sopracitati gli scienziati sono al lavoro per lo sviluppo di altre tipologie di batterie, si sta lavorando su una tipologia fatta da ioni di alluminio, ma la tecnologia è ancora ai primi sviluppi. La richiesta di energia dell’uomo è sempre maggiore, per questo occorrono batterie con una potenza maggiore e le aziende produttrici di batterie sono sempre alla ricerca di nuove tecnologie.